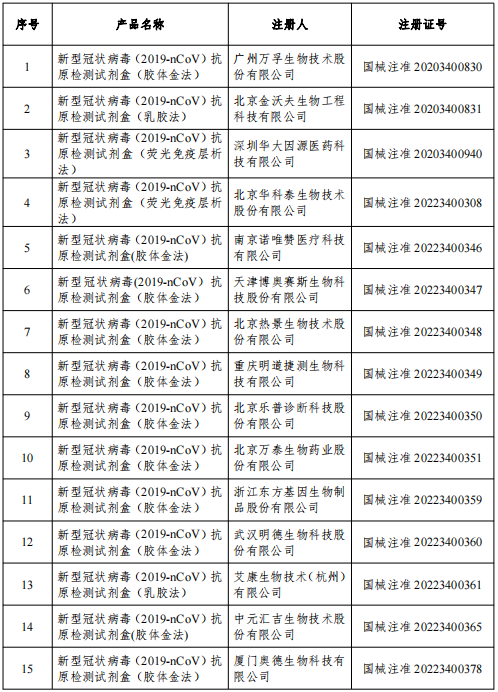
人民网北京12月22日电 (记者孙红丽)据国家药监局官网消息,12月22日,经国家药监局审查,批准艾维可生物科技有限公司和迈克生物股份有限公司的2个新冠病毒抗原检测试剂产品。截至目前,国家药监局已批准44个新冠病毒抗原检测试剂产品。 国家药监局表示,药品监督管理部门将加强相关产品上市后监管,保护患者用械安全。 资料显示,根据疫情防控工作需要,为进一步保障新冠疫情防控用抗原检测试剂供应,国家药监局于12月8日发布《关于延长新冠病毒抗原检测试剂注册证有效期的公告》,将已获准注册的新冠病毒抗原检测试剂的注册证有效期,在原有效期基础上延长6个月,切实保障相关产品市场供应。 另外,12月9日,经国家药监局审查,批准佰奥达生物科技(武汉)股份有限公司、基蛋生物科技股份有限公司和泰普生物科学(中国)有限公司3个企业的3个新冠病毒抗原检测试剂产品。 12月11日,经国家药监局审查,批准中山生物工程有限公司的新冠病毒抗原检测试剂产品。
国家药监局已批准44个新冠病毒抗原检测试剂
2022-12-22 00:00:00来源: 人民网
赞
你的鼓励是对作者的最大支持
- 叶玲:当中医药事业推动者 做群众健康守护者2022-12-22 00:00:00
- 福建福州开通城市中心发热门诊一站式服务2022-12-22 00:00:00
- “阳了”之后怎么吃?官方食谱来了!2022-12-22 00:00:00
- 川西高原的古杨树2022-12-22 00:00:00
- 连环画的时代新变2022-12-22 00:00:00
- 看浙江油画百年风华2022-12-22 00:00:00
- 2022港澳视觉艺术双年展举行2022-12-22 00:00:00
- 学界聚焦中国叙事与世界华文文学2022-12-22 00:00:00
- 兰卡斯特大学图书馆的浪漫(阅读时光)2022-12-22 00:00:00
- 中国足协:各俱乐部应在12月31日前解决全部历史欠薪2022-12-22 00:00:00